-
Chương 1. Cân bằng hóa học

-
 Cân bằng hóa học
Cân bằng hóa học
- 1. Phản ứng thuận nghịch là gì? Cân bằng hóa học là gì?
- 2. Các yếu tố ảnh hưởng như thế nào đến cân bằng hóa học? Nguyên lí chuyển dịch Le Chatelier được phát biểu như nào?
- 3. Biểu thức hằng số cân bằng là gì? Có những yếu tố nào ảnh hưởng đến cân bằng hóa học?
- 4. Sự điện li là gì? Chất điện li là gì? Phương trình điện li là gì?
- 5. Thế nào là acid – base theo thuyết Bronsted – Lowry? Chất lưỡng tính là gì?
- 6. Tích số ion của nước là gì? Cách tính pH của dung dịch là gì?
-
-
Chương 2. Nitrogen. Sulfur

-
 Nitrogen
Nitrogen
-
 Sulfur
Sulfur
- 1. Sulfur dioxide có tính chất hóa học gì? Tại sao sulfur dioxide là khí gây ô nhiễm môi trường?
- 2. Tính chất vật lí của sulfur là gì? Sulfur thể hiện tính hóa học gì?
- 3. Công thức Lewis của sulfuric acid là gì? Tính chất hóa học của sulfuric acid đặc và loãng khác nhau như thế nào?
- 4. Một số muối sulfate thường gặp là gì? Dùng dung dịch gì để nhận biết ion SO42-?
-
-
Chương 3. Đại cương hóa học hữu cơ

-
Chương 4. Hydrocarbon

-
Chương 5. Dẫn xuất Halogen - Alcohol - Phenol

-
Chương 6. Hợp chất carbonyl - carboxylic acid

Khái niệm tích số ion của nước và thang pH
Tích số ion của nước là gì?
\({H_2}O \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {H^ + } + O{H^ - }\)
\({K_{\rm{w}}} = {\rm{[}}{{\rm{H}}^{\rm{ + }}}{\rm{][}}O{H^ - }{\rm{]}}\)
Ở 250C, \({K_{\rm{w}}} = {\rm{[}}{{\rm{H}}^{\rm{ + }}}{\rm{][}}O{H^ - }{\rm{]}}\)=10-14 (không đổi)
pH là gì? Cách tính pH của dung dịch?
Ph là đại lượng đặc trưng cho mức độ acid base của một dung dịch
Công thức tính: \(pH = - \lg [{H^ + }{\rm{]}}\)
Thang pH là gì?
pH có giá trị từ 1 đến 14
Với pH < 7 --> môi trường acid
pH > 7 --> môi trường base
pH = 7 --> môi trường trung tính
Chất chỉ thị pH là gì? Có mấy loại chất chỉ thị PH?
Chất chỉ thị pH để cho biết dung dịch có tính acid hay base.
Có nhiều loại chất chỉ thị, thường dùng như: giấy quỳ tím, phenolphthalein, methyl da cam.
Phương pháp chuẩn độ dung dịch acid và base là gì?
Là phương pháp xác định nồng độ của một chất trong dung dịch bằng một dung dịch khác đã biết nồng độ.
Muốn xác định nồng độ của dung dịch NaOH bằng dung dịch HCl đã biết nồng độ. Người ta tiến hành phương pháp chuẩn độ.
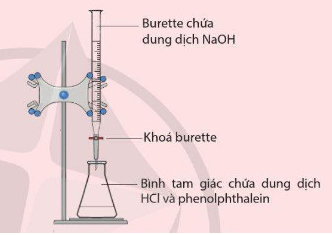
Sau khi chuẩn độ xong, ta có công thức: \({C_{{M_{NaOH}}}}.{V_{NaOH}} = {C_{{M_{HCl}}}}.{V_{HCl}}\)